
За две последние недели в молекулярной биологии случилось сразу два важных события, заполонивших новостные ленты. Во-первых, была определена последовательность генома неандертальца и выяснилось… ну, в общем, такое выяснилось… Но об этом в другой раз, а сейчас — про вторую сенсацию, «искусственную бактерию» Крейга Вентера (J. Craig Venter).
Подавляющее большинство комментариев в интернет-СМИ говорило о «бактерии из компьютера», «искусственной жизни» и тому подобных устрашающих — ну, или вдохновляющих — материях. Этому немало способствовал сам Вентер, в многочисленных интервью упиравший как на возможные биотехнологические приложения новой технологии, так и на философские проблемы. Что же все-таки было сделано, в чем состоит достижение и на каком участке пути к созданию бактерий с наперед заданными свойствами «с нуля» мы теперь находимся?
Пятнадцать лет назад, в октябре 1995 г., была определена последовательность генома паразитической бактерии Mycoplasma genitalium. Он составлял 580 тыс. пар нуклеотидов и содержал 480 белок-кодирующих генов. Это не рекорд — наименьший из опубликованных геномов, Carsonella rudii, имеет длину 160 тыс. пар нуклеотидов и кодирует 182 белка, но разница в том, что карсонелла может жить только внутри другой клетки (это эндосимбионт насекомых), а микоплазма может быть выращена в пробирке. Тогда же целый ряд ученых заинтересовался тем, а какой набор генов действительно минимален. Эту проблему можно изучать с двух сторон. Наши соотечественники Евгений Кунин и Аркадий Мушегян из Национального центра биотехнологической информации США, а потом и другие группы применяли биоинформатический подход, основанный на предположении, что если ген встречается во всех бактериях, он необходим. Параллельно развивались экспериментальные методы: гены разрушали случайными вставками и проверяли жизнеспособность полученных мутантов. В частности, в 1999 г. группа Вентера провела такой анализ для микоплазмы и показала, что около сотни ее генов не обязательны для роста в лабораторных условиях.
После этого Вентер поставил перед собой задачу создать бактерию с минимальным геномом. Для этого надо было решить целый ряд сложных технических задач. Использовать разрушение генов плохо: получится геном с минимальным набором генов, но большим количеством обломков, что неэкономично и некрасиво. Эффектнее и эффективнее казалось взять существующую бактерию, удалить из бактериальной клетки ее собственный геном, и вставить новый. Но для этого надо, чтобы новый геном заработал со старым аппаратом клетки — с него должны нормально считываться белки. И надо уметь синтезировать очень длинные фрагменты ДНК.
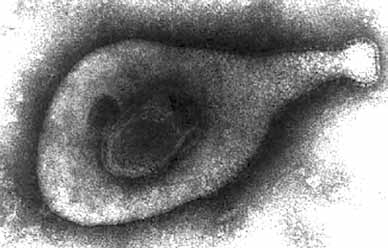
Оказалось, что работать удобнее с другой микоплазмой, Mycoplasma capricolum. Ее собственный геном больше, но это и не важно — он же все равно будет удален, — а растет она намного быстрее. Еще через четыре года Вентер с коллегами показал, что можно заменить геном M. capricolum на геном еще одной микоплазмы, M. mycoides. Полученная клетка нормально живет, а ее потомство после нескольких делений неотличимо от обычных M. mycoides, что и не удивительно — старые белки понемногу деградируют, а синтез новых белков определяется новым геномом.
Следующий шаг был сделан в 2008 г., когда исследователи синтезировали геном M. genitalium и вставили его обратно в клетку M. genitalium. Это нужно было для создания техники синтеза больших молекул ДНК и проверки того, что синтезированный геном так же работоспособен, как природный. Для контроля, чтобы отличить синтезированный геном от старого, авторы статьи закодировали в нем в неважных местах свои имена и адреса электронной почты.
В прошлом году эти две техники были объединены: та же процедура была проделана с клеткой M. capricolum и природным, но немного модифицированным, геномом M. mycoides. И, наконец, несколько дней назад Вентер с коллегами опубликовал статью про полностью искусственно синтезированный геном M. mycoides в клетке M. capricolum. Определив последовательность генома полученного организма, исследователи обнаружили несколько изменений — точечных замен, вставок и перестановок, произошедших в ходе сборки синтетического генома из фрагментов. На самом деле, таких ошибок синтеза было больше, причем одна из них, случившаяся в гене, необходимом для копирования генома, существенно задержала работу. Однако большинство ошибок было выявлено заранее, при проверке функциональности отдельных фрагментов, и остались только такие, которые не влияют на работу генов.
Итак, сделан очередной важный шаг на пути создания искусственных геномов. Это, несомненно, очень красивая и технически сложная работа. Заслуживает ли она разразившейся шумихи? Видимо, все-таки нет. Ни о какой искусственной жизни с заранее заданными свойствами речи не идет. То, что геном одной бактерии работает в клетке другой, очень близкой, уже было показано ранее. То, что геном может быть синтезирован «с нуля» — тоже; к тому же, еще до работ Вентера с бактериями это было показано на вирусах. До практических приложений еще очень далеко. Более того, вообще говоря, не очевидно, почему с практической точки зрения этот подход лучше, чем уже давно разработанные и с успехом применяемые методы генной инженерии известных биотехнологических штаммов.
Ясно, что важную роль сыграла личность самого Крейга Вентера, человека, очень склонного к публичности и громким обещаниям, — и умеющего эти обещания выполнять, как он доказал работой по определению последовательности генома человека. Очень любопытно выглядит введение к последней статье — оно читается не столько как обзор, сколько как автобиография. И неудивительно: Вентер настолько опережает конкурентов, что просто нечего цитировать. И можно предположить, что уже через год или два появится статья про очередной шаг на пути к «минимальной бактерии», в синтезированном геноме которой будут отсутствовать гены, про которые из предыдущих работ известно, что без них можно обойтись.
А если говорить о настоящих «искусственных организмах», то следует вспомнить о работах Питера Шульца из Института Скриппса, который уже несколько лет успешно создает организмы с измененным генетическим кодом — не геномом, а именно кодом, то есть системой соответствий между ДНК и белками. Для этого конструируется специальная тРНК (молекула, которая доставляет аминокислоту к синтезируемому белку) и проводится «молекулярная эволюция» аминоацил-тРНК-синтетазы (белка, связывающего тРНК с нужной аминокислотой) так, чтобы она узнавала новую, отсутствующую в обычных белках аминокислоту. В результате клетка синтезирует белки с такой аминокислотой, что бывает очень полезно для изучения их структуры, функций и взаимодействий. Но вот шума вокруг этого почему-то куда меньше.
Михаил Гельфанд