
В 2019 году Нобелевскую премию по химии за вклад в создание литий-ионных аккумуляторов получили трое ученых — Акира Ёсино, Стэнли Уиттингем и Джон Гуденаф. Это событие, разумеется, всколыхнуло и обрадовало всю научную общественность, прямо или косвенно связанную с электрохимическими источниками тока в частности, и материаловедением вообще. В этой статье мы постараемся разобраться с двумя вопросами: во-первых, почему премию дали именно за литий-ионные аккумуляторы (ЛИА), а во-вторых, почему ее удостоились именно эти трое ученых.
Чтобы ответить на первый вопрос, достаточно взглянуть на свой мобильный телефон, планшет или ноутбук — те вещи, без которых нашу жизнь сложно представить (если вы живете, скажем, в Норвегии или Калифорнии, то можно еще взглянуть на парковку, но в России электромобили приживаются гораздо медленнее по целому ряду причин). Собственно, мобильная электроника была в 1990-х годах основным драйвером развития технологии ЛИА: объемная плотность энергии, которая значительно превышает этот показатель у предшественников, сыграла здесь решающую роль. Второй отраслью, быстро оценившей преимущества ЛИА, были космические предприятия и агентства. Здесь уже ориентировались больше на массовую плотность энергии и отличную циклируемость батарей при большой глубине разряда. Удельная плотность современных батарей на основе ЛИА составляет 150–200 Вт × ч / кг (для единичной ячейки приближается к 300 Вт × ч / кг), а аналогичный показатель для массовых предшественников — свинец-кислотных, никель-кадмиевых и никель-металлгидридных — составляет в среднем 40, 60 и 90 Вт × ч / кг соответственно. Таким образом, технология ЛИА действительно оказалась революционной, и если на рубеже XX и XXI веков революция затронула в основном мобильную электронику и космическую индустрию, то сейчас триумфальное шествие ЛИА перекинулось на электротранспорт и крупные системы генерации электроэнергии. Преимущества электротранспорта перед бензиновыми аналогами обсуждать, наверное, уже даже несерьезно, а что касается последней области — ЛИА являются наиболее эффективным и удобным способом сглаживания и согласовывания пиков выработки и потребления энергии для электростанций, относящихся к «альтернативной» энергетике — в основном речь идет о солнечных и ветряных станциях. Если раньше применение ЛИА в этой области сдерживалось высокой ценой за кВтч энергии, то снижение этого показателя до 200–300 долл. / кВтч дало толчок и этому рынку ЛИА.
Ответ на второй вопрос менее очевиден для широкой публики, но вполне понятен для специалистов. Конечно, проблемами ЛИА заняты тысячи ученых по всему миру, и многие из них внесли существенный вклад в развитие науки и технологии. Разумеется, невозможно как-то численно и абсолютно объективно оценить вклад каждого из них. Тем не менее, Нобелевский комитет сделал свой выбор, и обосновать его можно следующим образом.

Майкл Стэнли Уиттингем более всего известен тем, что инициировал саму концепцию литий-ионного аккумулятора. Он предложил катодный материал на основе дисульфида титана, структура которого сохранялась бы при многократном внедрении/извлечении катионов лития. Такой способ хранения носителей заряда отличается от предшествующих решений, где кристаллическая структура катода и анода не сохранялась в ходе заряда-разряда (этот механизм называют «конверсионным»). Преимущество интеркаляционного механизма — высокая удельная и объемная плотность энергии, малое изменение объема материала и крайне низкая деградация при многократном заряде-разряде — т. е. те самые отличия ЛИА, которые обеспечили успех технологии. Уиттингем создал прототип, но на тот момент не существовало интеркаляционного анода, поэтому противоэлектродом сульфиду титана служил металлический литий либо сплавы на его основе.

Следующим — в хронологическом порядке — открытием стал оксид кобальта и лития, предложенный Джоном Гуденафом в качестве катода. LiCoO2 обладал более высоким рабочим потенциалом по сравнению с дисульфидом лития и отличался еще большей плотностью энергии и лучшей циклируемостью. Примечательна сама идея использования оксида в качестве интеркаляционного катода — до этого считалось, что связи Li—O слишком прочны и литий не будет обладать высокой подвижностью в оксидных материалах. Неудивительно, что новаторскую идею предложил именно Гуденаф — он фактически является отцом всей современной химии твердого тела, и спектр его научных интересов и достижений гораздо шире области ЛИА. Собственно, из всей троицы лауреатов Гуденафа можно назвать наиболее заслуженным: по некоторым данным, 97-летнего ученого многократно номинировали на премию в течение последних десятилетий, однако по разным причинам обходили. Возвращаясь к оксиду LiCoO2, можно упомянуть, что Гуденаф попал в самую точку: сегодня, почти сорок лет спустя после выхода статьи в Materials Research Bulletin (кстати, это самая цитируемая статья в журнале), кобальтат лития до сих пор используется примерно в 30% ЛИА. Еще 40% используют оксиды, производные от LiCoO2, — Li(Ni, Mn, Co)O2
или Li(Ni, Co, Al)O2. Оставшиеся проценты делят между собой постепенно уходящий в прошлое LiMn2O4 и набирающий популярность LiFePO4 — и здесь мы снова возвращаемся к Гуденафу. Дело в том, что в 1997 году, когда технология ЛИА уже вовсю завоевывала свое место под солнцем, Гуденаф выдвинул еще одну идею, показавшуюся многим спорной: использовать фосфат лития-железа в качестве катодного материала. Спорность идеи заключается в том, что в «анионных», или «полианионных» соединениях, к которым относится LiFePO4, электропроводность на несколько порядков ниже, чем у оксидов. Кроме того, в структуре оливина (характерной для LiFePO4) скорость диффузии лития также крайне низка. Таким образом, сразу после выхода этой статьи в Journal of the Electrochemical Society (и здесь, кстати, публикация является наиболее цитируемой в журнале) никакой масштабной реакции в научной или технологической среде не последовало. Разразилась она спустя несколько лет, когда другая группа ученых синтезировала LiFePO4 в форме наночастиц, покрытых углеродом, — это позволило решить проблему и низкой электропроводности, и медленной диффузии лития в материале. После этого мир кинулся осваивать и развивать тематику полианионных катодов. Их основным преимуществом стала повышенная безопасность, что для многих применений является критичным фактором. Так, аккумуляторы с катодом на основе LiFePO4 очень достойно проходят тесты на «протыкание» (симуляция механического повреждения) и перезаряд (симуляция ошибки системы управления, приводящая к слишком сильному увеличению напряжения). Если ЛИА на основе оксидов возгораются в обоих случаях, что иногда приводит к трагическим последствиям, то аккумуляторы на основе LiFePO4 в большинстве своем просто перестают работать. Кроме того, катоды на основе LiFePO4 способны заряжаться и разряжаться за считанные минуты (и даже меньше) и выдерживать десятки тысяч циклов заряда-разряда без существенной потери емкости.
Подытоживая вклад Гуденафа в технологию ЛИА, можно сказать, что он стал основателем всего «катодного» семейства аккумуляторов, хотя, повторюсь, его вклад гораздо шире: работы Гуденафа во многом определили облик всей современной химии твердого тела и материаловедения.

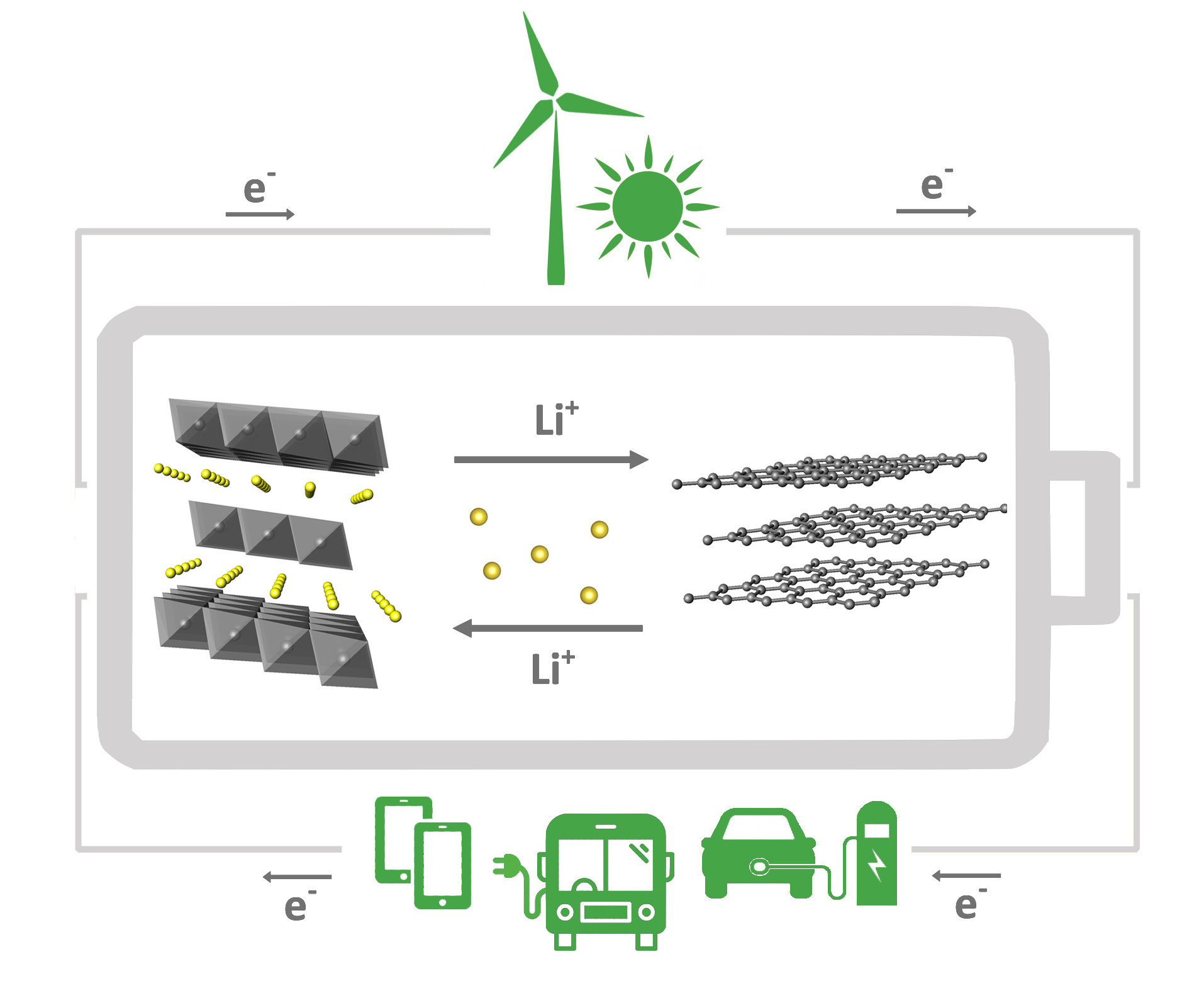
Для полноты картины нам необходимо понять, в чем же заключается вклад третьего ученого — Акиры Ёсино. Для этого нужно вернуться в 1980-е годы и вспомнить, что к этому моменту имелась концепция литий-ионного аккумулятора и катод, способный к обратимому извлечению/внедрению катионов лития. Дело осталось за анодом, обладающим тем же свойством. Акира Ёсино предложил такой анод — углерод. Если быть точным, первым рассмотренным вариантом был так называемый soft carbon — графитизируемый углерод. Впоследствии он трансформировался сначала в hard carbon — неграфитизируемый углерод, а затем в графит. Литий в этих материалах встраивается в межслоевое пространство графита (на каждое шестичленное кольцо приходится один катион лития, т. е. предельный состав — LiC6), а также «прикрепляется» к концевым атомам или дефектам в случае разупорядоченных графитоподобных элементов, существующих в hard carbon или soft carbon. Акира Ёсино, создавший недостающий кусок пазла, создал и само устройство — собственно прототип литий-ионного аккумулятора. Отличие «литий-ионного» от «литиевого» заключается именно в обратимой интеркаляции/деинтеркаляции катионов лития в оба главных компонента аккумулятора — катод и анод. Этот механизм назвали rocking chair — кресло-качалка. Открытие Акира Ёсино приблизило коммерциализацию ЛИА, и в 1991 году компания Sony выпустила первую партию аккумуляторов с катодом на основе LiCoO2 и углеродным анодом.
На сегодняшний день ЛИА остаются наиболее эффективными, долговечными и удобными в эксплуатации электрохимическими источниками тока. Существует ряд концепций, превосходящих ЛИА в плотности энергии, — например, литий-воздушные или литий-серные аккумуляторы, — но, несмотря на десятилетия активных исследований, этим системам так и не удалось обеспечить достаточный уровень циклируемости и выйти на массовый рынок. Возможно, человек, который сможет решить проблемы в этих или других альтернативных системах, станет когда-нибудь очередным нобелевским призером, но на сегодняшний день технология-лауреат не имеет конкурентов. Одна из особенностей ЛИА — потрясающая гибкость системы в плане оптимизации всех компонентов — катода, анода, электролита и т. д. Многим знакомы такие понятия, как «литий-титанатный аккумулятор» (ЛИА с анодом на основе литий-титановой шпинели), «литий-полимерный аккумулятор» (ЛИА с полимерным электролитом, хотя в последнее время чаще всего этими словами обозначают аккумуляторы с обычным жидким электролитом в мягком полимерном корпусе), «феррофосфатный аккумулятор» (ЛИА с катодом на основе LiFePO4) и т. д. Эта практически бесконечная вариативность позволяет ЛИА успешно развиваться и занимать всё новые и новые ниши и рынки.
Олег Дрожжин,
канд. хим. наук, ст. науч. сотр. химического факультета МГУ